단계 성장 중합


단계 성장 중합(Step-growth polymerization)은 이작용기 또는 다작용기가 이량체, 삼량체, 올리고머, 최종적으로 긴 고분자 사슬을 형성하는 고분자화 메커니즘의 종류 중 하나이다. 폴리에스테르, 폴리아마이드, 폴리우레탄 등과 같은 많은 자연발생 폴리머 및 몇몇의 합성 폴리머는 단계 중합을 통해 만들어진다. 높은 정도의 분자량을 얻기 위해서 중합 메커니즘의 특성상 반응의 진행 정도가 완전에 가까운 수준의 반응이 요구된다. 단계 중합 메커니즘은 사람들이 두 팔(=반응 부위)을 편 채로 손을 맞잡아 길게 연결된 사슬의 모양으로 이해할 수 있다. 단량체의 반응 부위는 작용기가 두개 이상존재할 수 있는데, 세개 이상일 경우 고분자가 가지 달린 형태로 자라날 수 있다.
IUPAC의 경우 단계 중합이란 단어를 사용하지 않는다. 대신 전파단계가 첨가반응이며, 첨가반응에서 분자가 성장하지 않는 경우 첨가중합(Polyaddition), 전파단계가 축합 반응이고 과정 중 성장하는 경우 축합 중합(Polycondensation)의 단어 사용을 권장한다.
축합 중합(condensation polymerization)[편집]
단계 중합과 축합 중합은 서로 다른 두개의 개념으로 비슷하지만 항상 같지는 않다. 일례로 폴리우레탄은 고분자를 제외한 분자가 추가적으로 형성되지 않기 때문에 첨가 중합임을 알 수 있지만, 반응 메커니즘은 단계 중합에 해당한다.
첨가중합과 축합중합은 1929년 Wallace Carothers에 의해 생산물 유형에 따라 구분되었다.[2][3]
- 단일 고분자(첨가)
- 고분자와 작은 분자량의 분자(축합)
Carothers의 분류 이후 일부 첨가중합은 전형적인 축합 중합의 특성을 갖는 것이 확인되어 더 이상 정확하지 않아 새로운 분류체계를 고안해냈다.
단계중합과 사슬중합은 1953년 Paul Flory에 의해 반응 메커니즘에 따라 구분되었다.[4]
- 작용기에 의한 중합 (단계 중합)
- 자유 라디칼 또는 이온에 의한 중합(사슬 중합)
사슬 중합과의 차이[편집]
| 단계 성장 중합 | 사슬 성장 중합 | |
|---|---|---|
| 중합도 | 서서히 증가 | 초기 높은 중합도 |
| 단량체 소모 속도 | 반응 초기 빠른 소모 | 반응 속도가 느리며 긴 시간 후에도 남아있음 |
| 반응 단계 | 전반에 걸쳐 유사 단계 반복 | 개시, 전파, 종료 및 연쇄전달의 각 단계별 다른 방식 사용 |
| 평균 분자량 | 초기에는 천천히 증가하지만 높은 반응 정도에서 급격히 증가 | 초기 단계에서 빠르게 증가한 후 중합반응 전반적으로 거의 동일하게 유지 |
| 후 활성 상태 | 계속 성장(반응성 유지) | 사슬 성장 후 반응성 소실 |
| 개시제 필요성 | 필요 없음 | 필요 |
단계 중합 폴리머의 종류[편집]

폴리에스터(polyester)[편집]
폴리에스터(polyester)는 높은 유리전이온도(glass transition temperature) Tg와 용융점 Tm을 가지고 있다. 약 175°C까지 본래의 물리적 성질을 유지할 수 있고 용매 및 화학 물질에 대한 내성이 있다. 폴리에스터는 섬유 또는 필름형태로 쓰인다. 전자는 의류, 펠트, 타이어 코드 등에 사용되며 후자는 자기식 기록 테이프와 고급 필름에 사용된다.
폴리에스터는 크게 2가지 양식으로 단계중합반응에 의해 합성 될 수 있다. 첫번 째로 카복실산을 가지는 물질과 알콜 작용기를 가지는 물질을 단위체로 합성될 수 있다. 하나의 단위체로도 합성이 될 수 있는데 이 경우, 그 단위체에 알코올과 카복실산 작용기를 모두 포함하고 있어야한다.[7]
폴리아미드(polyamide)[편집]
아미드(나일론)는 고강도, 우수한 탄성 및 내마모성, 우수한 인성, 유리한 내용제성 등의 좋은 균형의 성질을 갖추고 있다. 로프, 벨트, 섬유 천, 스레드, 베어링의 금속 대체, 전선 상의 재킷 등에 사용된다.
폴리아미드는 폴리에스터와 합성방법이 유사하다. 알코올 작용기 대신에 아민기로 대체하여 합성을 하면 폴리아미드를 얻을 수 있다.[8]
폴리우레탄(polyureathane)[편집]
폴리우레탄은 내마모성, 경도, 그리스에 대한 내성 및 탄성이 좋은 탄성중합체(elastomer)로 사용된다. 게다가 폴리우레탄은 여러 형태로 사용할 수 있다. 반발력이 우수한 섬유와 용제 공격 및 마모에 대한 내성이 우수한 코팅으로 사용할 수 있다. 또한 강도, 반발력 및 충격 강도가 우수한 폼으로 사용할 수 있다.
열경화성 수지는 아니나 유사한 3차원 구조를 가진 플라스틱이다. 질기고 화학약품에 잘 견디는 특성을 가지고 있다. 전기절연체, 구조재, 기포단열재, 기포쿠션, 탄성섬유 등에 사용되며, 신축성이 좋아서 고무의 대체물질로도 사용된다.
아이소시아네이트기(-N=C=O)는 쉽게 수산기(-OH)와 결합한다 (우레탄 결합). 이 반응을 이용하여 다이아이소사이아네이트에 수산기 둘을 가진 분자를 반응시키면 선상고분자(線狀高分子)가 된다.

폴리우레아(polyurea)[편집]
폴리우레아는 높은 Tg를 가지고 있으며 윤활유, 기름 및 용매에 대한 적절한 내성을 가지고 있다. 트럭의 베드 라이너, 교량 달의 코팅, 균열의 메꾸기 및 장식 디자인에 사용할 수 있다. 최근에는 이산화탄소를 줄이는 동시에 폴리우레아를 합성하는 방법이 만들어졌다. 1,6-hexanediamine에 를 이용하여 2단계 중합반응을 진행한다. 최종생성물은 열적으로 매우 안정하여 265°C에 용융점을 가지며 300°C에 분해된다.[9]

폴리실록산(polysiloxane)[편집]
폴리실록산은 여러 가지 물리적 형태로 쓰인다. 액체로 시작해서 윤활유, 왁스, 수지 및 고무의 형태로 쓰인다. 소포제 및 이형제, 개스킷, 씰, 케이블 및 와이어 절연, 고온 액체 및 가스 도관 등으로 쓰인다. 폴리실록산은 Dicholorocialkylsilane의 가수분해를 통해 합성할 수 있다. 실리콘에 알킬기가 붙어 있는데 종류가 바뀔 수 있다. 이는 얻고자는 물질의 물리적 특성에 따라 결정할 수 있다.[11]
폴리카보네이트(polycarbonate)[편집]

폴리카보네이트는 투명한 자기 소화성 물질이다. 그들은 결정성 열가소성, 높은 충격 강도, 우수한 열 및 산화 안정성과 같은 특성을 가지고 있다. 그들은 기계, 자동차 산업 및 의료 응용 분야에서 사용할 수 있다. 예를 들어, F-22 Raptor의 조종석 캐노피는 광학 품질이 우수한 폴리카보네이트로 만들어졌다. 폴리카보네이트는 염기성 용액에서 비스페놀A(bisphenol A)와 아실화 염소(acyl chloride)의 축합반응에 의해 합성된다. 비스페놀A를 수산화소듐 용액과 함께 만든 후 유기용매에 아실화염소를 녹인 후 이를 합친다. 이 두 용액의 계면에서 중합반응이 진행되어 폴리카보네이트를 합성한다.[12]
폴리설파이드(polysulfide)[편집]
폴리설파이드는 유기성 물질과 용매에 대해 우수한 저항성을 가지고 있으며 기체 불투과성, 오존과 산화에 대한 저항성을 가지고 있다. 그러나 냄새가 심하고 인장강도가 낮고 내열성이 약하다. 가솔린 호스, 개스킷 및 용매저항성 및 가스 저항성이 요구되는 장소에 쓰인다.
폴리에테르(polyether)[편집]
폴리에테르는 우수한 열가소성 거동, 수용성, 일반적으로 우수한 기계적 특성, 적당한 강도 및 강성을 나타낸다. 면, 합성섬유의 크기조절, 접착제용 안정제, 바인더, 의약품의 필름 형성제에 쓰인다.
페놀-포름알데히드 수지(베이클라이트)[편집]
페놀 포름알데히드 수지 (베이클라이트)는 내열성, 치수 안정성 및 대부분의 용매에 대한 내성이 우수하다. 유전(流電)적 특성도 좋다. 그에 따라 전기, 라디오, 텔레비전 및 자동차 부품의 성형 응용 분야에 쓰인다. 다른 용도로 함침지, 바니시, 벽 덮개용 장식 라미네이트에서 쓰인다.
폴리트리아졸 중합체(Polytriazole polymers)[편집]
폴리트리아졸 중합체는 알킨 및 아지드 작용기를 모두 보유하는 단량체로부터 생산된다. 단량체 간에는 이것은 azide-alkyne Huisgen cycloaddition이라고도 불리는 1,3-dipolar cycloaddition에 1,2,3-트리아졸기를 중심으로 연결되어 있다. 그 결과로 중합체는 강한 수지 또는 겔의 형태로 존재한다.[13][14]말단 알킨 및 말단 아지드를 함유하는 올리고펩티드를 단량체로 가지는 클릭된 펩티드 중합체는 펩타이드 효소의 작용으로 생분해될 것이다.[15]
가지고분자[편집]
3개 이상의 작용기를 가지는 단량체는 fractional conversion이 낮음에도 불구하고 서로 교차결합된 네트워크 형태의 중합체를 형성할 것이다. 물질 내에서 나뭇가지와 같은 위상을 가지는 지점을 gel point라고 하는 바, 물질의 점액성의 급격한 변화로 감지할 수 있다. 최초의 소위 열경화성 물질 중 하나는 베이클라이트로 알려져 있다. 단계적 성장 중합에서 항상 물이 방출되는 것은 아니다. 비환식 디엔 복분해 또는 ADMET 디엔은 중합 시 ethene을 소실한다.
역학[편집]
단계 중합 반응의 동역학 및 속도는 폴리에스테르화 메커니즘을 이용하여 설명할 수 있다. 에스테르화는 산과 알코올과의 상호작용을 통해 에스테르와 물을 생성하는 산 촉매 과정이다. 이때 운동 모델을 설명하기 위해서는 다음 세 가지의 가정이 필요하다.
1. 에스테르와 함께 생성된 물 또는 다른 부산물이 효율적으로 제거되어야 한다.
2. 작용기 반응성은 사슬 길이와는 상관이 없다.
3. 반응에서 각 단계는 하나의 알코올과 하나의 산만을 포함하는 것으로 가정한다.
이는 일반적인 폴리에스터화 n차 반응의 중합도이다.
자가 촉매 폴리에스테르화[편집]
산 촉매가 첨가되지 않은 경우에도 산이 자체 촉매로 작용할 수 있기 때문에 반응은 계속 진행된다. 임의의 시간 t에서의 응축 속도는 -COOH 작용기가 소모되는 속도로부터 도출될 수 있다.
COOH항이 2차인 이유는 산이 자가 촉매로 사용되기 때문에 생성되며, k는 속도 상수이다. 동일한 양의 산과 글리콜을 가진 시스템의 경우, [COOH]=[OH]이므로 작용기의 농도는 다음과 같이 간단히 쓸 수 있다.
Carothers 방정식의 적분 및 치환 후, 최종 형태는 다음과 같다.
자기 촉매 시스템의 경우, 수 평균 중합도(Xn)는 √t에 비례하여 증가한다.[16]
외부 촉매 폴리에스테르화[편집]
촉매가 없이 진행되는 반응의 속도는 다소 느리다 또한 높은 Xn이 쉽게 얻어지지 않는다. 촉매의 존재 하에서, 속도의 가속이 존재하며, 운동식은 다음과 같이 변화한다[17]
각 작용기에 대하여 1차항이다. 이런 이유로, 식을 정리하면 다음과 같이 정리할 수 있다.
그리고 이를 적분하면
외부 촉매 시스템의 경우, 평균 중합도(Xn)은 t와 비례하여 증가한다.
그러나 위와 같이 carothers’ 이론을 이용하여 평균 중합도를 구한 경우 실제 측정되는 값보다 더 크게 측정된다. 이는 평균 중합도 무한대로 증가하기 전에 젤화가 먼저 일어나기 때문이다.[18]
선형 중합에서 분자량 분포[편집]
중합 생성물은 분자량이 다른 고분자 분자들의 혼합물이다. 이론적이고 실용적인 이유들로 중합시 분자량의 분포를 알아보는 것이 중요하다. 분자량분포(MWD)는 Flory에 의해 고안된 방법 기능기가 모두 동등한 반응성을 갖는 것을 가정한 통계학적인 접근이다.
확률[편집]
단계 성장 중합은 무작위 과정이므로 통계를 사용하여 시간 또는 변환의 함수로 x-단량체가 있는 사슬을 찾을 확률을 찾을 수 있다.
반응에 있어 반응도(Extent of reaction) p는 (반응한 작용기의 개수/초기에 존재하던 작용기 개수)로 확인할 수 있다.[19]
A 작용기가 x-단량체를 형성하며 반응했을 확률
반응하지 않은 작용기의 확률
방정식 결합시 시간 t일 때의 존재확률 Px는 다음과 같다.
여기서 Px는 무작위 조성 속 분자가 정확히 x단량체 단위를 선택할 확률로 몰분율임을 알 수 있다. x가 증가할수록 확률은 감소한다.
수 분율 분포 (Number fraction distribution)[편집]

수분율 분포는 모든 시스템에서 x-단량체의 분율이며 용액에서 찾을 확률과 같다.
Nx는 x-단량체의 개수, N은 반응 중 존재하는 총 고분자 분자의 개수이다.[20]
무게 분율 분포[편집]
무게분율 분포는 시스템에서 x-단량체의 분율과 질량 분율로 x-단량체를 찾을 확률이다.[1]
x-단량체의 무게분율 Wx는 중합도가 x인 분자의 총질량 / 모든 분자의 질량로 나타난다.

선형 고분자에 대한 무게분율 분포 그래프 그래프1, p=0.9600; 그래프2, p=0.9875; 그래프3, p=0.9950; - Mo는 반복단위의 몰질량
- No는 단량체의 초기 개수
- N 은 아직 반응하지 않은 작용기 수
Carothers 방정식에 대입
PDI[편집]
그러나 단계 성장 중합의 경우 Carothers 방정식을 사용해 다음과 같이 표현할 수 있다.
단계중합의 경우 높은 값의 p를 가져야 유용한 고분자가 형성되어 PDI값은 2에 접근한다.
선형 중합에서의 분자량 조절 (Molecular weight control in linear polymerization)[편집]
화학량론적 제어 필요성 (Need for stoichiometric control)[편집]
중합에서 분자량의 조절에 관한 두 가지 중요한 측면이 있다. 고분자의 합성에서 고분자의 성질은 보통 분자량에 크게 의존하기 때문에, 매우 특정한 분자량의 생성물을 얻는 데 관심이 있다. 원하는 중량보다 높거나 낮은 분자량도 마찬가지로 바람직하지 않다. 중합도(degree of polymerization)는 반응 시간의 함수이므로 적절한 시간에 반응을 급랭(quenching)함으로써 원하는 분자량을 얻을 수 있다. 다만, 이러한 방법으로 얻어진 고분자는 고분자 분자의 말단이 서로 더 반응할 수 있는 작용기를 포함하기 때문에 분자량의 변화를 초래한다는 점에서 불안정하다.
이러한 상황은 두 단량체의 농도가 근소하게 비화학량론적(nonstoichiometric)이도록 조정함으로써 방지할 수 있다. RA2 + RB2 중합에서 어느 한쪽의 단량체가 매우 약간의 과량만 되더라도 그 과량의 단량체에서 얻어지는 작용기들만으로 고분자 사슬이 끝나게 되기 때문에 중합도를 현저하게 감소시킨다(예를 들어 RB2가 과량이라면, 최종적으로 말단기 양쪽은 B가 된다).[21] 이 작용기들은 서로 반응할 수 없기 때문에 더 이상의 중합은 불가능하며, 사슬이 성장할 수 없어 고분자는 이후의 분자량 변화에 안정하다.
원하는 분자량을 달성하는 또 다른 방법은 단일작용기 단량체(monofunctional monomer), 즉 작용기가 하나만 있는 단량체를 소량 첨가하는 것이다. 흔히 연쇄 정지제(chain stopper)라 불리는 단일작용기 단량체는 이작용기 단량체(bifunctional monomer)의 중합을 조절하고 제한하는데, 이는 성장 중인 중합체가 작용기가 없는 사슬 말단을 생성하기 때문에 추가적인 반응을 할 수 없기 때문이다.[22]
정량적 측면 (Quantitative aspects)[편집]
고분자 분자량을 적절히 조절하기 위해서는 이작용기 단량체 또는 단일작용기 단량체의 화학량론 불균형을 정밀하게 조정해야 한다. 비화학량론적 불균형이 너무 크다면 고분자 분자량이 너무 작아질 것이다. 반응물의 화학량론적 불균형이 분자량에 미치는 정량적 효과를 이해하는 것이 중요하다. 또한, 이는 초기 반응 혼합물에 존재할 수 있거나 바람직하지 않은 부반응에 의해 형성될 수 있는 반응성 불순물의 정량적 효과를 알기 위해 필요하다. 작용기가 A 또는 B인 불순물은 이들의 존재를 정량적으로 고려하지 않는 한 고분자 분자량을 급격히 낮출 수 있다.[22] 보다 유용하게는, 혼합물 내 반응물의 정밀하게 조절된 화학량론적 불균형이 원하는 결과를 제공할 수 있다. 예를 들어 산염화물에 대한 다이아민의 과잉은 결국 산염화물이 완전히 소비되었을 때 더 이상 성장할 수 없는 두 개의 아민 말단기를 가진 폴리아마이드를 생성한다. 이는 캐러더스 방정식(Carothers equation)의 연장선에서 다음과 같이 표현할 수 있다.
여기서 은 단량체 불균형(stoichiometric imbalance)를 의미한다. 만약, 와 의 중합반응의 초기단계에 존재하는 및 의 작용기의 수를 각각 및 라고 하면,
여기에서, 은 1과 같거나 작다(물론 일 때는 제외).
단일작용기를 갖는 단량체가 분자량 조절을 위하여 부가된다면 어떠한 상황이 될 것인가에 대해 고찰해본다면, 에 대한 정의로부터 이들은 군임에 분명하다. 그러면, 불균형 요소는 아래와 같이 정의된다.
여기에서 은 첨가된 단일기능 분자 의 수를 나타낸다. 분자량 제한에 있어, 각 단일작용기인 분자가 과잉의 단량체와 동일한 정량적 효과를 가지기 때문에 앞에 계수 2가 필요하다. 은 위 식에서의 을 치환한 것이다.
지금까지 논한 내용은 및 를 갖는 반응에 대한 것이다. 형에서는 이며, 분자량은 단일작용기 반응물(monofunctional reagent)을 추가함으로써 구해진다. 의 정의를 제외하면, 동일한 관계식이 적용되며 는 언제나 와 동일하다.[23][24]
다중 사슬 중합[편집]
작용기를 세 개 갖는 단량체는 중합에 3개의 작용기가 참여할 수 있다. 이는 중합체에 가지를 만들어 궁극적으로 가교가 형성된 고분자를 형성할 수 있다. 이는 3차원적 3D 망상구조가 형성되는데 이 때 형성되는 지점을 겔 포인트라고 한다. 이 지점에서는 급격한 접도변화가 나타난다. 보다 일반적인 기능 인자 fav 는 다중 사슬 중합에 대해 단량체 단위당 존재하는 작용기의 평균수로 정의된다. 처음에 N0분자를 포함하고 두개의 기능 그룹 A와 B의 동일한 수를 포함하는 시스템의 경우 작용기의 총 수는 N0fav이다.
이후 carothers 방정식을 통해 나타내면[25]
이 때 p는 다음과 같다.
단계 중합 고분자의 발전 (Advances in step-growth polymers)[편집]
새로운 고분자의 설계는 가벼운 내열성 고분자로 금속과 같은 재료들을 대체할 수 있다는 가능성에 의해 진행된다. 경량 고분자는 장점인 고강도, 내용제성 및 내화학성을 이용해 자동차 및 항공기의 전자 부품과 엔진 부품의 제조, 조리 도구 코팅, 마이크로 전자 부품과 전자 부품의 회로 기판 제작 및 코팅 용도 등으로 사용된다. 방향족 화합물 기반, 큰 분자량 또는 많은 가교를 가진 고분자 사슬은 높은 결합 강도와 강성이라는 특징을 가진다. 사슬 뼈대에 방향족이 있는 고분자는 방향족의 딱딱함과 안정성으로부터 기인한 높은 기계적 물성과 내열성, 내방사선성을 가지는 경향이 있다. 중축합으로 제조되는 중요한 방향족 고분자에는 방향족 폴리설파이드, 방향족 폴리이미드 등이 포함된다.[26] 한편으로, 강한 쌍극자 간 결합, 수소 결합 상호작용 및 결정성은 내열성을 향상시킨다.
원하는 기계적 강도를 얻기 위해서는 충분히 큰 분자량이 필요하지만, 분자량 증가에 따라 용해도가 감소한다는 문제가 생길 수 있다. 이는 적절한 단량체 혹은 공단량체를 유연한 결합으로서 강성 결합 사이에 포함시켜 해결할 수 있다. 또는 기능성 말단부를 포함하는 반응성 텔레켈릭 올리고머를 이용할 수 있다. 올리고머의 중합반응은 사슬 연장이라는 방식을 통해 더 큰 분자 만드는 데 기여한다.[27]
방향족 폴리에테르 (Aromatic polyether)[편집]

구리 염과 아민의 촉매 복합체를 사용하여 제작한, 2,6번에 치환기를 갖는 페놀의 산화적 결합 중합은 방향족 폴리에테르를 형성하는데, 이는 상업적으로 폴리 페닐렌 옥사이드(p-페닐렌 옥사이드) 또는 PPO라고 불린다. 단순 PPO는 용융점도가 높아 상업적으로 사용하기 어렵다. PPO와 고강도 폴리스타이렌(HIPS)를 혼합하면 가공성 및 인성이 개선된다.[28]
폴리에테르설폰 (Polyethersulfone)[편집]

폴리에테르설폰(PES)은 방향족 디할라이드와 비스페놀레이트 염 사이의 친핵성 방향족 치환에 의해 합성된다. 폴리에테르설폰은 부분적으로 결정성이며, 광범위한 수성 조건 및 유기 환경에 대한 높은 내성을 갖고 있다. 240~280°C의 온도에서 연속적인 사용이 가능하다. 가장 내열성이 좋은 열가소성 수지이다.[29]
방향족 폴리설파이드 (Aromatic polysulfides)[편집]
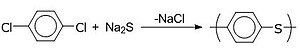
폴리 페닐렌 설파이드(p-페닐렌 설파이드, PPS)는 1-메틸-2-피롤리디논(NMP)과 같은 극성 용매에서 황화나트륨과 p-디클로로벤젠의 반응에 의해 합성된다. 이는 기본적으로 내염성이며 유기 및 수성 조건에 대해 안정적이지만 산화제에 다소 민감하다. PPS는 자동차, 전자레인지 부품 용도로 사용되기도 하고, 플루오르화 탄소 고분자와 혼합하여 조리도구용 코팅 용도로 사용되거나 밸브, 파이프, 전지 등을 보호하는 코팅에 사용한다.[30] 이외에도 혼합용, 성형용으로 사용된다.[26]
방향족 폴리이미드 (Aromatic polyimide)[편집]

방향족 폴리이미드는 이무수물과 다이아민의 반응에 의해 합성된다. 예를 들어, 피로멜라이트 무수물과 p-페닐렌다이아민의 반응으로 합성된다. 한편 디아민 대신 디이소시아네이트를 사용하여 합성할 수 있다. 용해성을 고려하여 이무수물 대신에 이무수물의 하프 산-하프 에스테르를 사용할 수 있다. 중합은 폴리이미드의 불용성으로 인해 2단계 공정으로 진행된다. 첫 번째 단계에서 NMP 또는 N,N-다이메틸아세트아미드와 같은 극성 비양성자성 용매를 이용해, 용해성 고분자량 폴리아민산을 형성한다. 두 번째 단계에서 폴리아미산을 최종 고분자 제품(필름, 섬유, 라미네이트, 코팅)의 형태로 처리할 수 있으며, 이는 용해되지 않고 융해되지 않는다. 필름, 코팅, 접착제, 적층화 용도로 사용된다.[26]
텔레켈릭 올리고머 접근법 (Telechelic oligomer approach)[편집]
텔레켈릭 올리고머 접근법은 중합 중 올리고머(분자량이 50-3000 정도) 단계에서 중합을 멈추게 하기 위해, 단일 작용기 반응물을 제외하는 방식이다. 단일 작용기 반응물은 중합을 제한할 뿐만 아니라 올리고머의 경화를 달성하기 위해 후속 반응이 가능한 작용기로 올리고머의 말단을 막는다. 알카인, 노보넨, 말레이미드, 아질산염, 시안산염과 같은 작용기가 이를 위해 사용된다. 말레이미드 및 노르보르넨으로 끝이 막힌 올리고머는 가열에 의해 경화된다. 알킨, 니트릴 및 시안산으로 끝이 막힌 올리고머는 방향족 구조를 생성하는 사이클로트리머화를 겪을 수 있다.
참고 문헌[편집]
- ↑ 가 나 Cowie JM, Arrighi V (2008). 《Polymers: Chemistry and Physics of Modern Materials》 3판. CRC Press.
- ↑ Carothers, Wallace H. (1929년 8월). “STUDIES ON POLYMERIZATION AND RING FORMATION. I. AN INTRODUCTION TO THE GENERAL THEORY OF CONDENSATION POLYMERS”. 《Journal of the American Chemical Society》 (영어) 51 (8): 2548–2559. doi:10.1021/ja01383a041. ISSN 0002-7863.
- ↑ Flory, Paul J. (1953). 《Principles of polymer chemistry》. Ithaca, N.Y. ISBN 0-8014-0134-8.
- ↑ Selke, Susan E. M. (2004). 《Plastics packaging : Properties, processing, applications, and regulations》 2판. Munich, Germany: Hanser Pub. 29쪽. ISBN 1-56990-372-7.
- ↑ Seymour, Raymond B. (1992). 《Polymer chemistry : an introduction》 3, rev. a expa판. New York: M. Dekker. ISBN 0-8247-8719-6.
- ↑ Platzer, Norbert (1988년 3월). “Encyclopedia of polymer science and engineering, 2nd ed., by Mark Bikales Overberger Menges, Wiley-Interscience, New York, 1987, 840 pp. Price: $200.00”. 《Journal of Polymer Science: Polymer Letters Edition》 26 (3): 169–170. doi:10.1002/pol.1988.140260314. ISSN 0360-6384.
- ↑ Young, Robert J. (2011). 《Introduction to polymers》 3판. Boca Raton: CRC Press. 23쪽. ISBN 978-0-8493-3929-5.
- ↑ Young, Robert J. (2011). 《Introduction to polymers》 3판. Boca Raton: CRC Press. 23쪽. ISBN 978-0-8493-3929-5.
- ↑ Jiang, Shan; Shi, Ruhui; Cheng, Haiyang; Zhang, Chao; Zhao, Fengyu (2017년 10월 1일). “Synthesis of polyurea from 1,6-hexanediamine with CO2 through a two-step polymerization”. 《Green Energy & Environment》 (영어) 2 (4): 370–376. doi:10.1016/j.gee.2017.05.001. ISSN 2468-0257.
- ↑ “Polysiloxanes”. 2022년 6월 4일에 확인함.
- ↑ Young, Robert J. (2011). 《Introduction to polymers》 3판. Boca Raton: CRC Press. 27-28쪽. ISBN 978-0-8493-3929-5.
- ↑ “Polycarbonates” (영국 영어). 2022년 6월 4일에 확인함.
- ↑ Wan, Liqiang; Luo, Yonghong; Xue, Lian; Tian, Jianjun; Hu, Yanhong; Qi, Huimin; Shen, Xuening; Huang, Farong; Du, Lei (2007년 4월 15일). “Preparation and properties of a novel polytriazole resin”. 《Journal of Applied Polymer Science》 (영어) 104 (2): 1038–1042. doi:10.1002/app.24849.
- ↑ Li, Yujing; Wan, Liqiang; Zhou, Hao; Huang, Farong; Du, Lei (2013). “A novel polytriazole-based organogel formed by the effects of copper ions”. 《Polymer Chemistry》 (영어) 4 (12): 3444. doi:10.1039/c3py00227f. ISSN 1759-9954.
- ↑ Dijk, Maarten van; Nollet, Maria L.; Weijers, Pascal; Dechesne, Annemarie C.; Nostrum, Cornelus F. van; Hennink, Wim E.; Rijkers, Dirk T. S.; Liskamp, Rob M. J. (2008년 10월 13일). “Synthesis and Characterization of Biodegradable Peptide-Based Polymers Prepared by Microwave-Assisted Click Chemistry”. 《Biomacromolecules》 (영어) 9 (10): 2834–2843. doi:10.1021/bm8005984. ISSN 1525-7797.
- ↑ Gnanou, Yves (2008). 《Organic and physical chemistry of polymers》. Hoboken, NJ: Wiley-Interscience. ISBN 0-470-23811-9.
- ↑ Cowie, J.M.G.; Arrighi, Valeria (2007년 7월 27일). “Polymers”. doi:10.1201/9781420009873.
- ↑ Young, Robert J. (2011). 《Introduction to polymers》 3판. Boca Raton: CRC Press. 49쪽. ISBN 978-0-8493-3929-5.
- ↑ Young, Lovell (2013년 2월 28일). 〈3〉. 《고분자과학》 3판. 자유아카데미. 28-33쪽. ISBN 978-89-7338-673-4.
- ↑ Stockmayer, Walter H. (1952년 7월). “Molecular distribution in condensation polymers”. 《Journal of Polymer Science》 9 (1): 69–71. doi:10.1002/pol.1952.120090106.
- ↑ Young, Robert J. (2013년 2월 28일). 《고분자과학》 3판. 자유아카데미.
- ↑ 가 나 Odian, George G. (1991). 《Principles of polymerization》 3판. New York: Wiley. ISBN 0-471-61020-8.
- ↑ Stevens, Malcolm P. (1990). 《Polymer chemistry : an introduction》 2판. New York: Oxford University Press. ISBN 0-19-505759-7.
- ↑ Stevens, Malcolm P. (1997년 11월 30일). 《고분자 화학 입문》 1판. 자유아카데미.
- ↑ Carothers, Wallace H. (1936). “Polymers and polyfunctionality”. 《Transactions of the Faraday Society》 (영어) 32: 39. doi:10.1039/tf9363200039. ISSN 0014-7672.
- ↑ 가 나 다 Young, Robert J. 《고분자과학 (Introduction to polymers)》 3판. 자유아카데미.
- ↑ Rogers ME, Long TE, Turners SR. 《Synthetic methods in step-growth polymers》. Wiley-Interscience.
- ↑ Mittal, Vikas (2015). 《Manufacturing of Nanocomposites with Engineering Plastics》.
- ↑ McKeen, Laurence W (2006). 《Fluorinated Coatings and Finishes Handbook》.
- ↑ Walton, David; Phillip, Lorimer (2000). 《Polymers》. Oxford Univ Pr on Demand. ISBN 978-0-19-850389-7.


![{\displaystyle {\frac {1}{1-p^{n-1}}}=1+(n-1)kt[{\ce {COOH}}]^{n-1}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f40d7c3649f67e96e10edcd26e6fab23275516ae)
![{\displaystyle rate={\frac {-d[{\ce {COOH}}]}{dt}}=k[{\ce {COOH}}]^{2}[{\ce {OH}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e36e9f9e72374e37c029a720efe9cb5e244de56e)
![{\displaystyle rate={\frac {-d[{\ce {COOH}}]}{dt}}=k[{\ce {COOH}}]^{3}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c02467b42290958b886e503d42cab7b3882e6b9d)

![{\displaystyle {\frac {1}{(1-p)^{2}}}=2kt[{\ce {COOH}}]^{2}+1=X_{n}^{2}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/11bd2e3f368961bfa8f4002c38928e4755ed2cba)
![{\displaystyle {\frac {-d[{\ce {COOH}}]}{dt}}=k[{\ce {COOH}}][{\ce {OH}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2fa3c69f4aa3a4c9646018d505e9e189a22e56ab)
![{\displaystyle {\frac {-d[{\ce {COOH}}]}{dt}}=k[{\ce {COOH}}]^{2}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/40623a5a6ecd32d96f118b41e932c376ed8c47f2)
![{\displaystyle {\frac {1}{1-p}}=1+[{\ce {COOH}}]kt=X_{n}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8addf76f8424ddca5c944ab775c0d7186bf58703)






























